目前,糖尿病的治疗达标率仍不高,并发症的控制也不尽如人意。新的降糖药物胰升血糖素样肽-1(GLP-1)类似物的应用,将直面2型糖尿病(T2DM)治疗的多重挑战,为糖尿病治疗提供新途径。
一、T2DM治疗面临的挑战
1.如何阻止β细胞功能的进行性减退:
T2DM以胰岛素抵抗(IR)、β细胞功能失代偿为特征。β细胞功能进行性减退在T2DM发生发展中起关键作用。T2DM的进程可分为5个阶段[1],在这5个阶段中,β细胞的数量、形态和功能发生着演变。在第1阶段中,为代偿IR,机体通过增加β细胞数量来满足胰岛素需要量的增加,以维持正常血糖水平。此时,血糖水平正常。尽管一些β细胞肥大,但其功能基本正常。第2阶段为轻度失代偿期,表现为血糖水平的轻度升高,空腹血糖超过116 mg/dL,胰岛素1相分泌严重缺乏,但2相分泌功能部分保存 。 虽然患者在这一糖尿病前期阶段可维持数年,但只要β细胞数量不足以代偿,血糖就会快速升高。第3阶段血糖的波动导致β细胞功能进一步降低和胰岛素分泌的减少。第4个阶段空腹血糖可以大于285 mg/dL,β细胞的凋亡增加,导致β细胞数量减少约50%,此时β细胞的功能和数量仍能维持相当一段时间,以分泌足够的胰岛素来避免代谢完全失代偿情况如严重高血糖和酮症的发生。第5阶段为严重的失代偿期,β细胞严重衰竭并可能出现酮症。
UKPDS研究显示,在T2DM发生发展过程中,β细胞功能进行性降低[2]。患者被诊断为T2DM时,胰岛β细胞功能已丧失超过50%,并以每年18%的速度继续下降,药物治疗控制血糖的效果也逐渐下降。2008年Banting奖获得者De Fronzo最近提出,β细胞功能的衰退远比人们预想的要早得多[3],即使是糖耐量受损(IGT)者,其β细胞功能也已丧失约80%。UKPDS研究还证实, 无论采用饮食干预、二甲双胍还是磺脲类药物,β细胞衰竭速度均相似。也正是由于β细胞功能的持续衰竭,T2DM患者单独使用任何一种口服降糖药物进行治疗都不能完全有效,随着时间的推移,即使药物不断强化直至使用胰岛素,也仍然难以长期稳定控制血糖。
由此可见,保护胰岛β细胞功能在T2DM治疗中至关重要。然而现有的治疗方案对如何有效阻止β细胞功能的衰退尚缺少有效对策,因而难以长期稳定控制血糖。
2.如何解决治疗达标和低血糖之间的矛盾:
血糖治疗达标无疑是延缓和降低糖尿病大血管和微血管并发症的重要手段。但随着血糖治疗达标率的提高,低血糖的发生率也随之增加。如何在血糖控制达标的同时减少低血糖及其相伴的体重增加是T2DM治疗面临的重要挑战之一。
血糖控制是降低糖尿病并发症的关键。现有单种药物治疗很难使大部分患者的血糖达标并长期维持。旨在评价全球糖尿病控制情况及指南依从性的国际研究——IDMPS第2阶段的结果显示,在8个国家4312例T2DM患者中,仅32.7% 达到HbA1c<7%,提示多数T2DM患者HbA1c及空腹血糖未达标。我国T2DM患者的长期血糖达标率仅为25%。医生和患者对治疗相关的体重增加和低血糖风险的担忧是血糖治疗达标的主要障碍之一。
低血糖一直是糖尿病治疗中困扰医患的难题,可能导致严重心脑血管意外乃至危及生命。Cryer等[4]指出:一次严重的医源性低血糖或由此诱发的心血管事件可能会抵消一生维持血糖在正常范围所带来的益处。 Enrique等对14670例冠心病患者随访8年的结果显示,低血糖可增加全因死亡率和癌症死亡率。Ming Wei等在一项纳入40069例研究对象的前瞻性队列研究中发现,低空腹血糖患者的心血管疾病死亡风险比血糖正常者增加2.7倍,全因死亡相对风险增加2倍。2008年的ACCORD研究也显示,严重低血糖与死亡发生风险相关[5],VADT试验也发现低血糖可以预测心血管原因死亡[6]。
3.如何全面控制危险因素使糖尿病患者更多收益:
对于T2DM高血糖的成因,过去人们所熟知的仅有胰岛β细胞的分泌缺陷、肝糖原输出增加和肌肉组织葡萄糖摄取减少这三方面。事实上,还有更多的组织器官参与了糖尿病的病理生理过程,包括:(1)脂代谢紊乱;(2)肠促胰岛素效应减弱;(3)胰岛α细胞分泌GLP增多;(4)肾小管对葡萄糖的重吸收增加;(5)下丘脑对血糖的调控紊乱。De Fronzo将所有这些影响T2DM高血糖形成的因素称为糖尿病生理病理“八重奏”[3]。“八重奏”进一步揭示了T2DM病理生理的复杂性,为临床用药带来了新的思考。
随着糖尿病治疗方案的日益优化,糖尿病患者生存期逐渐延长,由糖代谢异常所致的靶器官损害成为了影响患者预后的主要因素。糖尿病治疗目标也从单纯降糖变为保护靶器官,防止各种微血管和大血管并发症,尤其是心脑血管事件。众所周知,除糖代谢异常外,还有很多危险因素与心脑血管事件独立相关,包括超重、高血压、血脂异常等。面对这些挑战,人们一直在不断探索一种既可以保护β细胞功能,又能在有效降糖的同时针对其他病理生理缺陷,改善其他代谢紊乱,甚至保护心血管的T2DM治疗新思路。
二、GLP-1的应用前景
基于肠促胰素(Incretin)的治疗是近年来T2DM治疗领域的热点。尤其是 GLP-1类似物的临床应用前景备受关注。GLP-1主要由小肠下段的L细胞合成,具有多种生物学作用[7](图1)。它可以作用于β细胞,增强β细胞的增殖和分化,减少其凋亡,促进β细胞再生和修复,增加β细胞数量,从而增强其反应性,进而增加葡萄糖浓度依赖性胰岛素释放。还可以作用于α细胞以葡萄糖浓度依赖性地降低GLP的水平,减少餐后GLP分泌, 进而减少肝糖元的分解而降低血糖水平。作为一种肠源性激素,GLP-1是在营养物质特别是碳水化合物的刺激下才释放入血的,其促胰岛素分泌作用呈葡萄糖浓度依赖性,这种葡萄糖浓度依赖性降糖特性是其临床应用安全性的基础与保障,从而避免了人们对可能造成的严重低血糖的担忧。有活性的GLP-1 通过GLP-1受体起作用。后者除在胰岛细胞表达外,还分布于心脏、中枢神经系统、肾、肺、胃、肠、垂体以及腹部迷走神经传入纤维的神经节,因此可能会产生降糖以外的作用。GLP-1作为一种厌食信号肽,调节摄食与体重。研究提示,GLP-1可作用于下丘脑,激活饱食感神经元,减少进食;同时也可作用于胃部,延缓胃排空,从而减轻患者体重,而这正是多数降糖药物所不具备的。 GLP-1减轻体重的同时可能发挥心血管保护作用。输注GLP-1可以减少心肌梗死的面积,这在动物模型和人体中都得到了证实。研究结果提示,GLP-1还可以改善内皮细胞功能,有降压、保护神经等功能[8]。
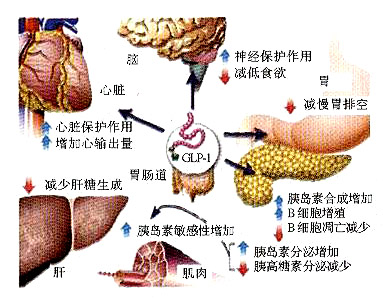
图1GLP-1在周边组织的直接与间接作用
GLP-1直接作用在内分泌胰腺、心脏、胃和脑部,间接作用在肝和肌肉
天然的GLP-1很容易降解,阻碍了其临床应用,由诺和诺德公司研制的GLP-1 类似物利拉鲁肽与人GLP-1的同源性高达97%,作用时间明显延长,只需每日注射一次,就发挥天然GLP-1的作用。其对β细胞的保护作用不仅在体外实验和动物实验中得到证实,也在T2DM患者中得到验证。利拉鲁肽无论是单药治疗还是与磺脲类药物、双胍类药物、TZD或胰岛素联合治疗,均有良好的降糖效果。不同剂量的利拉鲁肽单独或联合治疗能使T2DM患者的HbA1c较基线再降低1.0%~1.5%,同时使血糖达标率明显增加。多数降糖药物在治疗达标的同时常导致T2DM患者体重增加,而利拉鲁肽治疗的患者体重非但未增加,反而降低,尤其是对基线BMI较高的患者。LEAD系列研究显示,应用利拉鲁肽治疗的患者体重可较基线减少多达3.2kg[9]。利拉鲁肽在有效降糖并减轻体重的同时,还有望通过降低患者血压(可使收缩压降低2.7 -6.6mmHg)改善心血管危险。故利拉鲁肽的降压作用也颇具临床价值, 研究者们还在就利拉鲁肽的心血管作用进行新的探索。
T2DM复杂的病理生理机制使其治疗充满了挑战。GLP-1类似物以其独特的作用机制,同时作用于T2DM的多个病理生理靶点,在全面有效降低血糖的同时,减少低血糖的发生并减轻体重,同时对血压和心血管系统有潜在的益处,有望成为T2DM治疗的生力军。
参考文献
1.Weir GC, Bonner-Weir S. Five stages of evolving beta cell dysfunction during progression to diabetes. Diabetes,2004,53:S16-S21.
2.UK Prospective Diabetes Study Group.UK prospective diabetes study 16.Overview of 6 years’ therapy of type II diabetes: a progressive disease. Diabetes, 1995,44:12491258.
3.Defronzo RA, Banting Lecture. From the triumvirate to the ominous octet: a new paradigm for the treatment of type 2 diabetes mellitus. Diabetes, 2009,58:773795.
4.Cryer PE, Davis SN, Shamoon H. Hypoglycemia in diabetes. Diabetes Care,2003,26:1902-1912.
5.Gerstein HC,Miller ME,Byington RP, et al. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med, 2008,358:2545-2559.
6.Duckworth W ,Abraira C, Morits T, et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med,2009,360:129-139.
7.Drucker DJ. The biology of incretin hormones. Cell Metabolism,2006,3:154.
8.Baptist Gallwitz. New therapeutic strategies for the treatment of type 2 diabetes mellitus based on incretins. Rev Diabetic Stud,2005,2:61-69.
9.Alan J, Garber, Stephen J. An overview of incretin clinical trials. The Journal of Family Practice,2008,57:S10.
